前回のリトマス試験紙は植物等が持つpHで色が変わる色素を利用するの記事でリトマス試験紙はウメノキゴケ等の地衣類から得られた色素から出来ているという内容を記載した。
これを踏まえた上で、これから本題のpHメーターに入りたいところだけれども、今回は関係ある内容になるかわからないが一旦脱線する。
今回触れたいのは、中学校で習うボルタ電池だ。
ボルタ電池は銅、亜鉛と硫酸で構成されるが、今回は身近にあるレモンで見ていく。
※物理系は自信がないので、これは個人的なメモとして捉えて読み進めてほしい。

半分に切ったレモンに銅板と亜鉛板を指し、各々の板に電気を通す線で繋ぐ。
上の図のように途中で電球を配置すると配線が完成した時点で光る。
レモンは電気を通しつつ、有機酸が金属を溶かすので硫酸と同様の役割を果たす。
前提の話として、銅と亜鉛は、酸による溶けやすさは亜鉛 > 銅という特徴がある。
銅板と亜鉛板はどちらも金属で、酸に触れると
![]()
![]()
![]()
上のイラストのように水素イオンが金属から電子を奪い、金属は電子による繋がりが切られ溶ける。
上の図では電子は水素イオンが持っていってしまうが、今回の電池では電子は線を流れる。
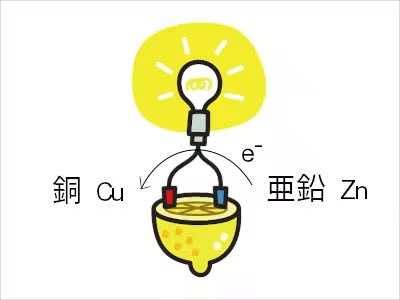
亜鉛の方が銅より溶けやすいので、亜鉛側の方の電子が余り、電子は移動しやすい線を流れることになる。
電子の流れはマイナス極(+極)からプラス極(−極)に流れるという紛らわしい状況になっているので、
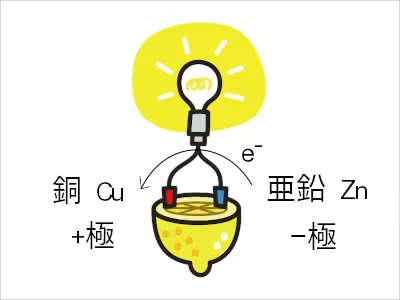
銅がプラス極になり、亜鉛がマイナス極になり電池が完成する。
プラス極の銅の方に電子が到達したら、pHを低くする要因である水素イオンが電子を持っていく。
これから出会う様々な測定器は今回の内容が基礎になるはずなので触れておいた。