タンパクの三次構造の際の結合:水素結合1でタンパク質を形成する際の結合方法である水素結合を記載した。
実際は三次構造形成以外でも使われているみたいだけど、そこはおいといて。
とりあえず、水素結合の話題を出したことだし、実際にどの様に結合されているかでもみてみよう。
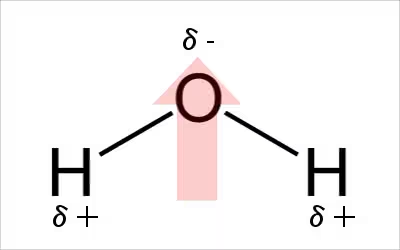
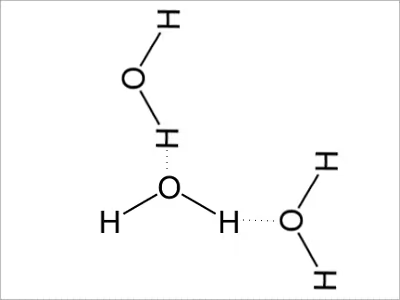
水素結合は電気陰性度の規則に従って極性をもった分子同士がつながりあうことで、
電気陰性度の規則に従っていれば、水分子でなくとも極性を持つ。
アミノ酸にも極性を持つものがいくつかあり、それがアスパラギンとセリンになる。
(上の二つは極性を持ちつつ、荷電を持たないもの。pHも中性。荷電をもち極性を持つアミノ酸はたくさんある)
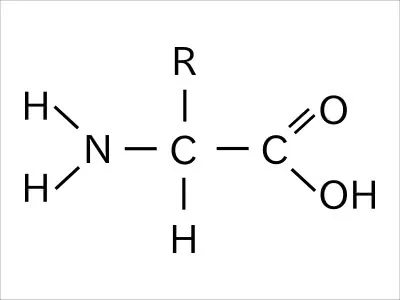
アスパラギンは、側鎖(R)がNH2COCH2のアミノ酸で、セリンは側鎖がCH2OHのアミノ酸になる。
このアミノ酸が向かい合うと、
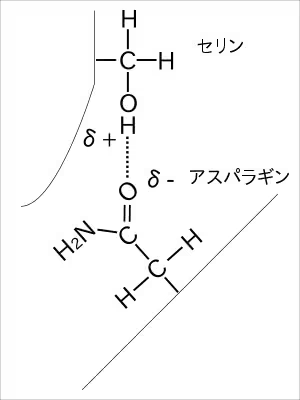
こんな感じで結合する。
アスパラギンの方のO=Cの箇所で酸素(O)が強い力で引っ張るのでδ-。
セリンの方はOHの箇所で、HがOに引っ張られるのでδ+。
この二つの極性で水素結合が発生するわけですね。
アミノ酸の側鎖でなくても、極性が発生する箇所はあるので、冒頭で記載したとおり、タンパクを形成する過程の至るところでこの結合は発生している。