稲作でケイ酸を効かせるにはどうすれば良いのか?の記事の投稿以降、ケイ酸について更に深い知識が必要だなと思い、改めてケイ酸についてを学ぶことにする。
目標は植物が利用できるシリカはどこにある?の記事で触れた各種造岩鉱物について、構造を考えながらどのように風化していくか?を考えられること。

(株式会社誠文堂新光社 日本の石ころ標本箱 201ページの図を参考にして作成)
造岩鉱物というのは、上の図の各種岩石を構成する鉱物を指し、岩石風化後の土質に大きく影響を与える可能性がある。
造岩鉱物にはケイ酸が含まれているものが多い。
はじめにケイ酸の構成元素を見ると、Siのケイ素とOの酸素でできている。
自然界ではSi単体では存在していないらしく、

酸素と結びついた形(例:石英 SiO2)で存在している。
いきなり余談だけれども、二酸化ケイ素(SiO2)を炭素(C)で還元すると、
SiO2 + C → Si + CO2
で単体のケイ素を得ることが出来る。
ケイ素は電気を通したり通さなかったりといった半導体の性質を持つため、コンピュータ産業で重要な位置付けになっているそうだ。
話は戻って、ケイ酸は極少量であるが水に溶ける。
nSiO2 + nH2O ⇄ nSi(OH)4
※100 μg/mL-1程度
ケイ酸とケイ酸塩の化学 ―シロキサン結合をもつ分子・粒子・ゲル― 化学と教育 66巻 1号(2018年)
Si(OH)4をモノケイ酸と呼び、植物の根ではモノケイ酸の形で吸収する。
ただ、モノケイ酸は弱酸性から中性の溶液内では、モノケイ酸のSi-OH(シラノール基)同士が反応してしまい、
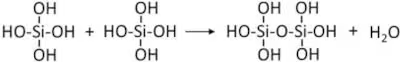
※図:ケイ酸とケイ酸塩の化学 ―シロキサン結合をもつ分子・粒子・ゲル― 化学と教育 66巻 1号(2018年)より引用
重合ケイ酸として大きな形としてなっていく。
ちなみにモノケイ酸同士の結合は上の図のように直鎖状(単鎖)になるわけではなく、
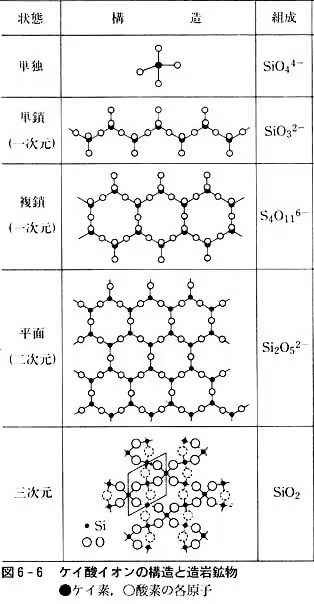
※表:放送大学 - 無機高分子 - ケイ酸塩 - 図6-6 ケイ酸イオンの構造と造岩鉱物の表を一部改変
のように複鎖のようになったりする。
ここらへんの知識が造岩鉱物の理解に必要になってくるそうだが、話が長くなったので今回はここまでにしておく。
余談
ケイ酸塩は熱水やアルカリ性の環境で溶けやすくなるそうだ。
おすすめのページ
2.鉱物 | 山口大学理学部 地球科学標本室・ゴンドワナ資料室