/** Geminiが自動生成した概要 **/
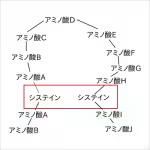
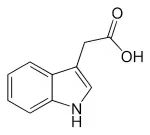
このブログ記事では、植物ホルモン「オーキシン(インドール酢酸:IAA)」と「腐植物質」の関連性を探ります。含窒素香気物質インドールの構造に着目し、神戸大学の研究論文を紹介。そこでは、オーキシンが腐植物質の超分子構造に保持され、pHやイオン強度の変化で放出されるメカニズムが示されています。この作用により植物の成長促進が期待でき、実際に植物がIAAを直接吸収する挙動も報告されています。さらに、土壌微生物もオーキシンを合成するため、腐植の定着と微生物の活性化が植物の発根促進に繋がると解説しています。