サリチル酸の角質軟化作用について3の記事で、
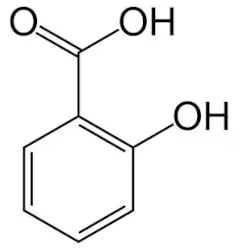
File:Aspirin-skeletal.svg originally by Benjah-bmm27 and Booyabazooka, edited by Fvasconcellos - File:Aspirin-skeletal.svg, パブリック・ドメイン, リンクによる
サリチル酸の化学的な特徴と、細胞膜の浸透について見た。
角質軟化作用を目的としたサリチル酸の使用で、細胞膜に浸透したサリチル酸は、次にタンパクや脂質に作用して角質層を軟化する。
今回はその内のタンパクに関して触れていく。
先にタンパクについておさらいしておく。
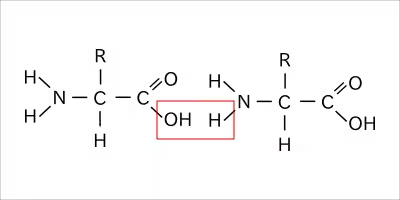
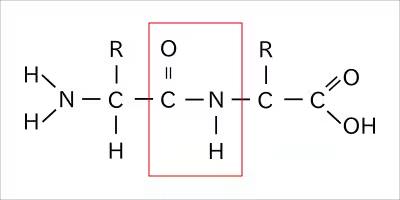
タンパクは20種類のアミノ酸がペプチド結合という反応で鎖状にアミノ酸が並ぶことによって構成される。
直鎖状に並んだアミノ酸の鎖はそれだけでは生理的な作用はなく、
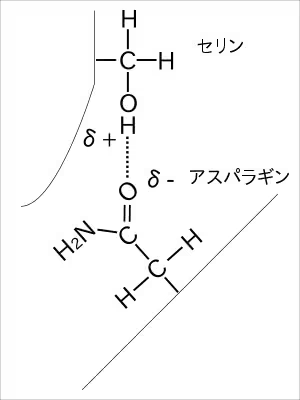
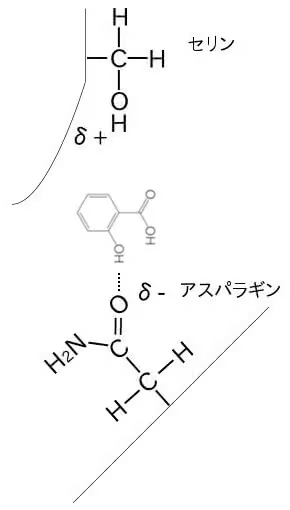
水素結合、
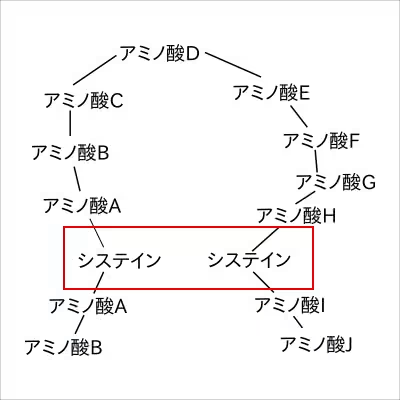

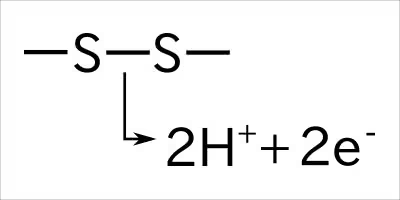
硫黄を持つアミノ酸同士のジスルフィド結合、極性を持つアミノ酸同士のイオン結合や、非極性のアミノ酸同士が隣り合う疎水性相互作用により
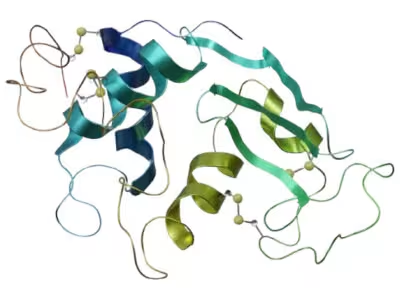
のような複雑に折り曲がった構造になり、化学的にたまたまできた隙間等に生理的な反応をする箇所があり、それが各々のタンパクの特徴となる。
たまたまできた隙間に生理的な作用を持つというのが重要で、この隙間は絶妙なバランスによって構成されているので、少しでもバランスを崩したら、本来持つタンパクの働きがなくなる(失活)。
タンパクにたどり着いたサリチル酸は、フェノール性ヒドロキシ基(上の図の右の-OH)がタンパクを形作る水素結合に入り込み、タンパクの形を少し変える。
この作用は消毒液としてのエタノールで見たエタノールの作用を同じだけれども、エタノールには角質軟化作用は期待できない。
サリチル酸とエタノールの大きな違いはベンゼン環を持つことで、ベンゼン環の非極性がタンパクのイオン結合と疎水性相互作用に影響を与え、タンパクの形を更に変える。
この二段階のタンパクの変成作用により、タンパクの持つ機能は大幅に変化する。
※変化する機能は生理的反応の他に水への溶けやすさもある。
追記
明確な記載は見つけていないが、タンパクの構造にサリチル酸が入ることにより、今までイオン結合をしていた箇所が外れ、これらの箇所は極性を持っていたため、タンパクの親水性が高まり、タンパク自身が水と結合しやすくなり、タンパク全体が軟化しやすくなったのでは?と考えている。